a
a-AMMINOACIDI:
STRUTTURA, SUDDIVISIONE E REATTIVITA’[E1][E1][E1][F1]
Struttura. Gli
a-amminoacidi
sono i monomeri che costituiscono le proteine. Essi sono tutti caratterizzati
dalla presenza della seguente coda della molecola:
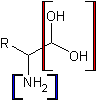
Il gruppo amminico è sempre legato al carbonio
a,
cioè al carbonio adiacente al gruppo carbossilico. Al carbonio
a di ogni
amminoacido sono sempre legati anche un atomo di idrogeno e una catena laterale
R. La rappresentazione riportata sopra è corretta dal punto di vista chimico, ma
non tiene conto delle condizioni imposte dall’ambiente in cui l’
a-amminoacido viene a trovarsi in
vivo: a pH fisiologico infatti il gruppo carbossilico è deprotonato, mentre il
gruppo amminico acquista un protone. Il risultato è la forma zwitterionica sotto
riportata:
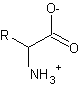
Suddivisione. Gli
a-amminoacidi
si distinguono tra loro in base alla catena laterale. In particolare si
distinguono: gli amminoacidi alifatici (glicina, alanina, valina, leucina,
isoleucina) in cui R rappresenta una catena alifatica o alchilica; gli
amminoacidi con catena laterale contenente zolfo o ossidrili (serina, cisteina,
treonina, metionina); gli amminoacidi aromatici (fenilalanina, tirosina,
triptofano) in cui R contiene un gruppo aromatico; gli amminoacidi basici (istidina,
lisina, arginina) che presentano gruppi basici nelle catene laterali; gli
amminoacidi acidi e le loro ammidi (acido aspartico, acido glutammico,
asparagina, glutammina) che presentano un gruppo carbossilico o ammidico nelle
catene laterali; esiste inoltre un a-amminoacido
ciclico (prolina).
Gli amminoacidi che costituiscono le diverse migliaia di
proteine sono quindi soltanto venti; dieci di questi sono sintetizzati dal
nostro organismo mentre gli altri dieci, gli amminoacidi essenziali,
devono essere assimilati tramite la dieta.
Gli amminoacidi sono generalmente indicati con insiemi di
tre lettere: ad esempio la glicina si indica con Gly, la lisina con Lys.
Reattività. Le reazioni degli
a-amminoacidi
sono quelle tipiche dei composti contenenti gruppi amminici e carbossilici;
inoltre tutti gli altri gruppi presenti sulla catena laterale possono dare le
loro reazioni caratteristiche.
Dall’interazione tra il gruppo amminico e quello
carbossilico di due a-amminoacidi
si forma il legame ammidico o peptidico (–NHCO–) caratteristico
dei composti chiamati peptidi.